
首批輝瑞新冠口服藥3200人份抵台!張上淳曝適用對象
Omicron本土疫情延燒,新冠口服藥採購與到貨進度備受矚目,今天傳出好消息!我國採購的輝瑞口服藥今天中午運抵台灣,有3200人份。張上淳表示,台灣目前已有2款新冠肺炎口服藥(輝瑞、莫納皮拉韋),是亞洲首位具備2款藥物的國家。療日子馬上帶您了解用藥資訊!
輝瑞新冠口服藥今抵台!2族群發病5天內適用,降低近9成死亡率
中央流行疫情指揮中心今(27)天表示,台灣向輝瑞藥廠採購的新冠肺炎口服藥於今天中午運抵台灣,數量有3200人份。指揮中心專家諮詢小組召集人張上淳說明,台灣是亞洲第二位取得這款口服藥的國家,只僅次於韓國。另外,由默沙東藥廠研發的新冠肺炎口服藥「莫納皮拉韋(Molnupiravir),台灣也在亞洲只僅次於日本取得。換句話說,台灣已有2款新冠口服藥,是亞洲首位具備2款藥物的國家。
張上淳表示,這款輝瑞口服藥取得食藥署的EUA授權並可緊急進口使用,專家諮詢小組也針對這款藥物的診治指引進行討論,清楚界定患者只要12歲以上、40公斤以上、未使用氧氣,且於發病5天內,具有任一重症風險因子都適用。
而「重症風險因子」的定義與默沙東藥廠研發的「莫納皮拉韋」的診治指引一致,包括年齡大於65歲、糖尿病、慢性腎病、心血管疾病、慢性肺疾、BMI大於25等其他影響免疫功能之疾病或已知重症風險。
此外,美國輝瑞藥廠在去年11月公布的臨床試驗結果顯示,旗下COVID-19輝瑞口服抗病毒藥物Paxlovid,可以將重症高風險患者的住院或死亡風險,大幅降低89%。輝瑞執行長博爾拉指出:「這些數據顯示,若獲得監管機構批准或授權,我們的口服抗病毒候選藥物可能挽救患者的性命,降低感染COVID-19的重症程度,並消除多達約90%住院治療。」

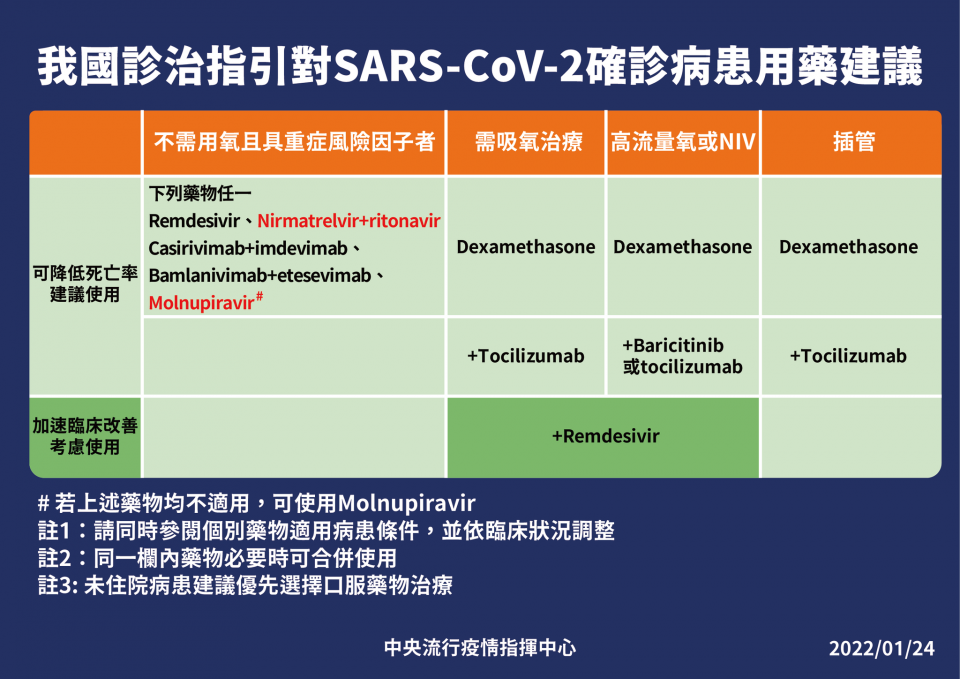
 ▲我國進口新冠肺炎口服藥Paxlovid診治指引與用藥建議。(圖/衛福部。)
▲我國進口新冠肺炎口服藥Paxlovid診治指引與用藥建議。(圖/衛福部。)
「莫納皮拉韋」口服藥須符合3條件 且須確實完成完整的5天療程
符合3條件可用藥:發病5天內、具有重症風險因子,且不適用其他治療選擇的輕度至中度COVID-19成人確診者,用藥後仍須依規定隔離。
食藥署指出,Molnupiravir適用於發病5天內、具有重症風險因子,且臨床上不適用其他治療選擇的成人輕度至中度COVID-19確診者。服用本藥品者應確實完成完整的5天療程,並於治療期間及治療結束後,依照嚴重特殊傳染性肺炎中央流行疫情指揮中心規定接受隔離,以提高病毒清除率,降低COVID-19傳播的可能性。此外,廠商應於專案核准輸入期間執行風險管理計畫,以保障病人用藥安全。但詳細使用指引仍待專家開會討論。

本文著作權屬療日子所有,非經取得著作權人同意不得任意修改、複製及轉載
默沙東口服藥防護效果30%,法國不買!副總裁:可對抗所有變異株包含Omicron
去年(2021)12月法國衛生部才因為默沙東口服藥「莫納皮拉韋」(molnupiravir)試驗數據並不符合預期,政府因此決定取消訂單。法國也因此成為全球首個放棄採用莫納皮拉韋的國家。
據《路透社》報導,默沙東研發副總裁、研究實驗室負責人李迪恩(Dean Li) 1月10日在摩根大通年度醫療會議上表示,「我們非常有信心,莫納皮拉韋的分子作用機制將對Omicron有效」,且預期可以對抗任何可能出現的變異株。
目前尚無數據證明莫納皮拉韋對Omicron效力,且根據默沙東去年11月公開對1433名患者的試驗數據,莫納皮拉韋降低住院及死亡風險的效果為30%,較先前公布的50%明顯降低。
莫納皮拉韋去年12月取得美國食品藥品監督管理局(FDA)及英國、日本、印度等國家授權,包括美國在內的多個國家都簽署採購協議。中央流行疫情指揮中心指揮官陳時中去年11月在立法院被問及新冠肺炎口服藥採購進度時也表示,已經完成簽約。
文章轉載自療日子-首批輝瑞新冠口服藥3200人份抵台!張上淳曝適用對象
